고객문의센터
Fax.044-862-8786
Email.
kk_cop@naver.com
kkcop@kakao.com
Keum-kwang Life Science
실험관련 소모자재 공급
생명공학화학 관련시약 및 실험검사측정장비
최고의 기술력과 다년간의 노하우로 고객 만족을 실현하는
믿음직한 기업으로 최선을 다할 것을 약속드립니다.
자료실
내용
최근 신경과학계의 떠오르는 분야는 광유전학(Optogenetics)이다. 광유전학은 빛으로 신경세포를 조절하는 첨단기술로, 빛에 민감한 단백질 유전자를 실험동물의 신경세포에 삽입해 빛의 파장에 따라 신경세포의 활성을 조절한다. 광유전학의 광 자극은 전기생리학을 적용한 전기 자극보다 좀 더 정교한 방법으로 신경세포들을 조절할 수 있다.
예를 들어 생쥐의 뇌를 비롯한 다른 동물들의 뇌는 깊숙이 파묻혀진 빛에 반응하지는 않는다. 과학자들은 빛에 반응하는 단백질에서 아이디어를 얻었다. 녹조류에는 채널로돕신2(Channelrhodopsin 2, 빛에 반응하는 단백질의 일종)라는 단백질이 있다. 이 단백질은 세포 표면에 위치하는 세포막 이온채널 단백질로, 빛에 따라 채널의 문을 열고 닫아 이온들이 세포 내로 들어오고 나가는 역할을 담당한다.
광유전학, 빛으로 신경세포 흥분 조절
2005년 미국 스탠포드대 칼 다이서로스(Karl Deisseroth) 연구팀은 채널로돕신2 단백질 유전자를 실험실 배양접시에서 자라고 있는 신경세포에 유전공학적으로 삽입했다.
이 신경세포에 푸른 빛의 파장을 비쳐주면 채널로돕신2 단백질의 채널이 열리게 되고 이 채널을 통해 양이온들이 신경세포 내부로 쏟아지면서 신경세포들은 흥분하게 된다. 즉 빛으로 신경세포의 활성을 조절한 셈이다.
신경세포는 기본적으로 세포막에 일정 수준의 전압을 띠고 있으며 이 전압을 다양하게 조절해 뇌 속의 복잡한 정보를 처리한다.
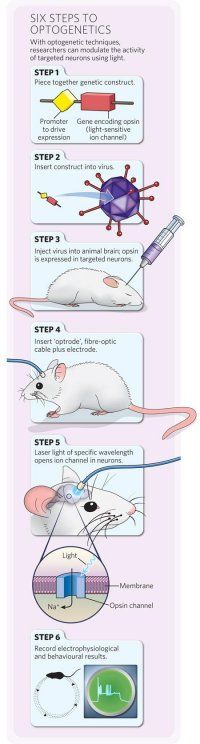
지난 5년 동안 광유전학 기술은 빠르게 발전했지만 기본적인 아이디어는 동일하다. 1단계는 빛에 민감한 단백질 유전자를 만드는 작업이다.
채널로돕신2 유전자나 옵신(Opsin)이라는 유전자가 대개 이용된다. 2단계는 이 유전자를 바이러스에 삽입한다.
바이러스는 이들 유전자를 실험동물의 신경세포에 전달하는 역할을 담당한다. 3단계로 바이러스를 실험동물의 뇌에 주입하면 바이러스는 광범위한 신경세포에 이들 유전자를 전달한다.
하지만 모든 신경세포에서 채널로돕신2 유전자가 발현하는 것은 아니다. 유전공학적으로 특정 신경세포에서만 발현하도록 조작했기 때문이다. 4계는 광섬유를 실험동물의 뇌에 연결한다.
5단계는 이 광섬유를 통해 특정 파장의 빛을 쏴주면 채널로돕신2 단백질이 반응하고 이에 따라 신경세포들이 반응한다. 마지막 6단계는 신경세포의 반응을 측정하고 기록하는 단계이다.
다이서로스 연구팀은 지난해 9월 광유전학 기술을 이용해 생쥐의 근육 움직임을 통제하는데 성공했다는 연구결과를 과학저널 ‘Nature medicine’에 게재했다. 연구팀은 채널로돕신2 단백질과 미세 LED 조각을 생쥐의 신경세포에 삽입했다. 이 생쥐에 빛을 쏴주자 생쥐의 다리 근육이 수축했다.
광유전학 기술 적용 근육수축 실험, 정상 반응에 가장 근접
근육은 작고 느리며 피로에 내성이 있는 근섬유와 크고 빠른 근섬유 등 두 종류의 근섬유로 구성된다. 작은 근섬유는 장기간에 걸쳐 정밀한 움직임을 조절하는데 이용되며 큰 근섬유는 순간적으로 큰 힘을 내는데 사용되지만 쉽게 피로해지는 경향이 있다.
인체에서 근육이 반응할 때 작은 근섬유가 먼저 활성화되고 큰 근섬유는 순간적인 힘과 속도를 위해 대기한다. 즉 작은 근섬유, 큰 근섬유 순서로 반응이 일어난다. 광유전학 기술을 적용하면 이들 섬유들은 정상적인 생리순서인 작은 섬유, 긴 섬유 순서로 활성화된다.
논문의 공동저자인 스탠포드대 스콧 델프(Scott Delp) 교수는 “적절한 자극으로 운동신경섬유의 자연적인 작동순서를 복구할 수 있었는데 이는 중요한 진전”이라고 말했다. 이전의 손상된 운동기능을 복구하려는 연구에서 전기 자극을 이용하면 큰 섬유가 작은 섬유보다 먼저 반응하는 경향을 보였다.
이는 근육수축이 잘못된 순서로 일어나는 것이고 그 결과로 절룩거리는 운동이 나타나고 쉽게 피로를 느끼게 되는 것이다. 광유전자 기술은 빛의 강도를 바꾸면 작은 섬유만을 활성활 수 있는데, 이는 전기 자극을 이용해서는 불가능한 방법이다.
과학자들은 빛으로 신경세포를 조절하는 광유전자 기술을 수년 내 신경세포의 손상으로 장애를 겪고 있는 중풍, 척추손상 등의 환자들에 적용할 수 있을 것으로 기대하고 있다. 장기적으로 빛에 민감한 단백질 유전자를 안전하게 삽입할 수 있는 기술이 개발되면 임상적용의 가능성도 그만큼 높아질 것으로 전망했다.
광유전학 인공망막, 외과적 이식보다 정밀한 시력 회복
광유전자 기술은 시력장애인들의 시력 회복에도 응용될 전망이다. 있다. 미국 웨일 코넬 의대 쉐일라 니렌버그(Sheila Nirenberg) 연구팀은 지난해 11월 맹인 생쥐가 사람이나 동물의 얼굴에서부터 센트럴파크의 복잡한 파노라마까지 거의 모든 이미지를 볼 수 있는 인공망막개발에 성공했다.
인공 망막은 현재도 존재하지만 눈 속 깊숙이 일련의 전극을 이식해야하는 외과수술을 필요로 한다. 이식된 전극은 시신경세포를 자극해 정보를 뇌로 전달하지만 외부적인 배터리를 필요로 하며 아주 어두운 곳에서 밝은 물체만을 대략적으로 식별할 수 있게 한다. 연구팀의광유전학 기술을 적용한 인공망막은 외과수술을 요구하지 않는다.
포유동물의 망막 속에는 빛을 감지하는 세포와 시각정보를 뇌에 전달하는 신경절 세포(Ganglian Cell)가 있다. 망막질환이나 노화에 따른 시력감퇴의 경우 빛 감지 세포는 소멸하나 신경절 세포는 정상적으로 생존한다. 시력장애를 연구하는 과학자들의 주된 연구대상 가운데 하나가 바로 이 신경절세포가 어떻게 흥분하는지 그 암호를 해독하는 것이다.
니렌버그 연구팀은 신경절 세포의 암호를 해독하면서 현존하는 전극을 이용하는 기술보다 보다 정교하게 시각정보를 뇌로 전달하는 방법을 연구했다. 연구팀은 광유전자 기술을 생쥐에 적용해 신경절 세포에 채널로돕신 단백질을 발현하도록 조작했다. 이후 연구팀은 생쥐에게 6천개의 진동 빛으로 구성된 격자로 해석되는 이미지를 보여줬다.
각각의 빛은 한 개의 신경절 세포와 반응해 신경세포의 흥분을 야기했으며 암호화된 이미지가 뇌에 전달됐다. 과학자들은 미래의 어느 시점이 되면 이러한 기술을 시력장애를 겪고 있는 인간에게도 적용할 수 있을 것으로 기대하고 있다.
광유전학을 인간의 뇌에 적용하기 위해서 필요한 기술 가운데 하나는 빛을 어떻게 하면 뇌의 깊숙한 곳에 위치한 신경세포에까지 전달하느냐이다. 현재 뇌의 깊숙한 곳까지 전기적 자극을 전달하는 전기자극기는 상품화돼 있다.
이 장비는 파킨슨질병과 같은 뇌질환에 사용이 허가돼 있다. 과학자들은 전기 대신 빛을 전달하는 비슷한 장비의 개발이 점진적으로 이뤄질 것이며, 이 기술가 자체 하나의 치료 요법이 될 것으로 전망했다.
우리나라의 경우 광유전학 분야의 세계적 석학 조지 어거스틴(George Augustine) 박사가 센터장을 맡고 있는 한국과학기술연구원(KIST) 기능커넥토믹스 센터 등을 중심으로 인간의 신경회로 기작 규명 및 관련 분야 신약 개발 연구에 박차를 가하고 있다.

최근 신경과학계의 떠오르는 분야는 광유전학(Optogenetics)이다. 광유전학은 빛으로 신경세포를 조절하는 첨단기술로, 빛에 민감한 단백질 유전자를 실험동물의 신경세포에 삽입해 빛의 파장에 따라 신경세포의 활성을 조절한다. 광유전학의 광 자극은 전기생리학을 적용한 전기 자극보다 좀 더 정교한 방법으로 신경세포들을 조절할 수 있다.
예를 들어 생쥐의 뇌를 비롯한 다른 동물들의 뇌는 깊숙이 파묻혀진 빛에 반응하지는 않는다. 과학자들은 빛에 반응하는 단백질에서 아이디어를 얻었다. 녹조류에는 채널로돕신2(Channelrhodopsin 2, 빛에 반응하는 단백질의 일종)라는 단백질이 있다. 이 단백질은 세포 표면에 위치하는 세포막 이온채널 단백질로, 빛에 따라 채널의 문을 열고 닫아 이온들이 세포 내로 들어오고 나가는 역할을 담당한다.
광유전학, 빛으로 신경세포 흥분 조절
2005년 미국 스탠포드대 칼 다이서로스(Karl Deisseroth) 연구팀은 채널로돕신2 단백질 유전자를 실험실 배양접시에서 자라고 있는 신경세포에 유전공학적으로 삽입했다.
이 신경세포에 푸른 빛의 파장을 비쳐주면 채널로돕신2 단백질의 채널이 열리게 되고 이 채널을 통해 양이온들이 신경세포 내부로 쏟아지면서 신경세포들은 흥분하게 된다. 즉 빛으로 신경세포의 활성을 조절한 셈이다.
신경세포는 기본적으로 세포막에 일정 수준의 전압을 띠고 있으며 이 전압을 다양하게 조절해 뇌 속의 복잡한 정보를 처리한다.
지난 5년 동안 광유전학 기술은 빠르게 발전했지만 기본적인 아이디어는 동일하다. 1단계는 빛에 민감한 단백질 유전자를 만드는 작업이다.
채널로돕신2 유전자나 옵신(Opsin)이라는 유전자가 대개 이용된다. 2단계는 이 유전자를 바이러스에 삽입한다.
바이러스는 이들 유전자를 실험동물의 신경세포에 전달하는 역할을 담당한다. 3단계로 바이러스를 실험동물의 뇌에 주입하면 바이러스는 광범위한 신경세포에 이들 유전자를 전달한다.
하지만 모든 신경세포에서 채널로돕신2 유전자가 발현하는 것은 아니다. 유전공학적으로 특정 신경세포에서만 발현하도록 조작했기 때문이다. 4계는 광섬유를 실험동물의 뇌에 연결한다.
5단계는 이 광섬유를 통해 특정 파장의 빛을 쏴주면 채널로돕신2 단백질이 반응하고 이에 따라 신경세포들이 반응한다. 마지막 6단계는 신경세포의 반응을 측정하고 기록하는 단계이다.
다이서로스 연구팀은 지난해 9월 광유전학 기술을 이용해 생쥐의 근육 움직임을 통제하는데 성공했다는 연구결과를 과학저널 ‘Nature medicine’에 게재했다. 연구팀은 채널로돕신2 단백질과 미세 LED 조각을 생쥐의 신경세포에 삽입했다. 이 생쥐에 빛을 쏴주자 생쥐의 다리 근육이 수축했다.
광유전학 기술 적용 근육수축 실험, 정상 반응에 가장 근접
근육은 작고 느리며 피로에 내성이 있는 근섬유와 크고 빠른 근섬유 등 두 종류의 근섬유로 구성된다. 작은 근섬유는 장기간에 걸쳐 정밀한 움직임을 조절하는데 이용되며 큰 근섬유는 순간적으로 큰 힘을 내는데 사용되지만 쉽게 피로해지는 경향이 있다.
인체에서 근육이 반응할 때 작은 근섬유가 먼저 활성화되고 큰 근섬유는 순간적인 힘과 속도를 위해 대기한다. 즉 작은 근섬유, 큰 근섬유 순서로 반응이 일어난다. 광유전학 기술을 적용하면 이들 섬유들은 정상적인 생리순서인 작은 섬유, 긴 섬유 순서로 활성화된다.
논문의 공동저자인 스탠포드대 스콧 델프(Scott Delp) 교수는 “적절한 자극으로 운동신경섬유의 자연적인 작동순서를 복구할 수 있었는데 이는 중요한 진전”이라고 말했다. 이전의 손상된 운동기능을 복구하려는 연구에서 전기 자극을 이용하면 큰 섬유가 작은 섬유보다 먼저 반응하는 경향을 보였다.
이는 근육수축이 잘못된 순서로 일어나는 것이고 그 결과로 절룩거리는 운동이 나타나고 쉽게 피로를 느끼게 되는 것이다. 광유전자 기술은 빛의 강도를 바꾸면 작은 섬유만을 활성활 수 있는데, 이는 전기 자극을 이용해서는 불가능한 방법이다.
과학자들은 빛으로 신경세포를 조절하는 광유전자 기술을 수년 내 신경세포의 손상으로 장애를 겪고 있는 중풍, 척추손상 등의 환자들에 적용할 수 있을 것으로 기대하고 있다. 장기적으로 빛에 민감한 단백질 유전자를 안전하게 삽입할 수 있는 기술이 개발되면 임상적용의 가능성도 그만큼 높아질 것으로 전망했다.
광유전학 인공망막, 외과적 이식보다 정밀한 시력 회복
광유전자 기술은 시력장애인들의 시력 회복에도 응용될 전망이다. 있다. 미국 웨일 코넬 의대 쉐일라 니렌버그(Sheila Nirenberg) 연구팀은 지난해 11월 맹인 생쥐가 사람이나 동물의 얼굴에서부터 센트럴파크의 복잡한 파노라마까지 거의 모든 이미지를 볼 수 있는 인공망막개발에 성공했다.
인공 망막은 현재도 존재하지만 눈 속 깊숙이 일련의 전극을 이식해야하는 외과수술을 필요로 한다. 이식된 전극은 시신경세포를 자극해 정보를 뇌로 전달하지만 외부적인 배터리를 필요로 하며 아주 어두운 곳에서 밝은 물체만을 대략적으로 식별할 수 있게 한다. 연구팀의광유전학 기술을 적용한 인공망막은 외과수술을 요구하지 않는다.
포유동물의 망막 속에는 빛을 감지하는 세포와 시각정보를 뇌에 전달하는 신경절 세포(Ganglian Cell)가 있다. 망막질환이나 노화에 따른 시력감퇴의 경우 빛 감지 세포는 소멸하나 신경절 세포는 정상적으로 생존한다. 시력장애를 연구하는 과학자들의 주된 연구대상 가운데 하나가 바로 이 신경절세포가 어떻게 흥분하는지 그 암호를 해독하는 것이다.
니렌버그 연구팀은 신경절 세포의 암호를 해독하면서 현존하는 전극을 이용하는 기술보다 보다 정교하게 시각정보를 뇌로 전달하는 방법을 연구했다. 연구팀은 광유전자 기술을 생쥐에 적용해 신경절 세포에 채널로돕신 단백질을 발현하도록 조작했다. 이후 연구팀은 생쥐에게 6천개의 진동 빛으로 구성된 격자로 해석되는 이미지를 보여줬다.
각각의 빛은 한 개의 신경절 세포와 반응해 신경세포의 흥분을 야기했으며 암호화된 이미지가 뇌에 전달됐다. 과학자들은 미래의 어느 시점이 되면 이러한 기술을 시력장애를 겪고 있는 인간에게도 적용할 수 있을 것으로 기대하고 있다.
광유전학을 인간의 뇌에 적용하기 위해서 필요한 기술 가운데 하나는 빛을 어떻게 하면 뇌의 깊숙한 곳에 위치한 신경세포에까지 전달하느냐이다. 현재 뇌의 깊숙한 곳까지 전기적 자극을 전달하는 전기자극기는 상품화돼 있다.
이 장비는 파킨슨질병과 같은 뇌질환에 사용이 허가돼 있다. 과학자들은 전기 대신 빛을 전달하는 비슷한 장비의 개발이 점진적으로 이뤄질 것이며, 이 기술가 자체 하나의 치료 요법이 될 것으로 전망했다.
우리나라의 경우 광유전학 분야의 세계적 석학 조지 어거스틴(George Augustine) 박사가 센터장을 맡고 있는 한국과학기술연구원(KIST) 기능커넥토믹스 센터 등을 중심으로 인간의 신경회로 기작 규명 및 관련 분야 신약 개발 연구에 박차를 가하고 있다.
 저작권자 2011.01.03 ⓒ ScienceTimes 저작권자 2011.01.03 ⓒ ScienceTimes |
0
0
게시물수정
게시물 수정을 위해 비밀번호를 입력해주세요.
댓글삭제게시물삭제
게시물 삭제를 위해 비밀번호를 입력해주세요.
